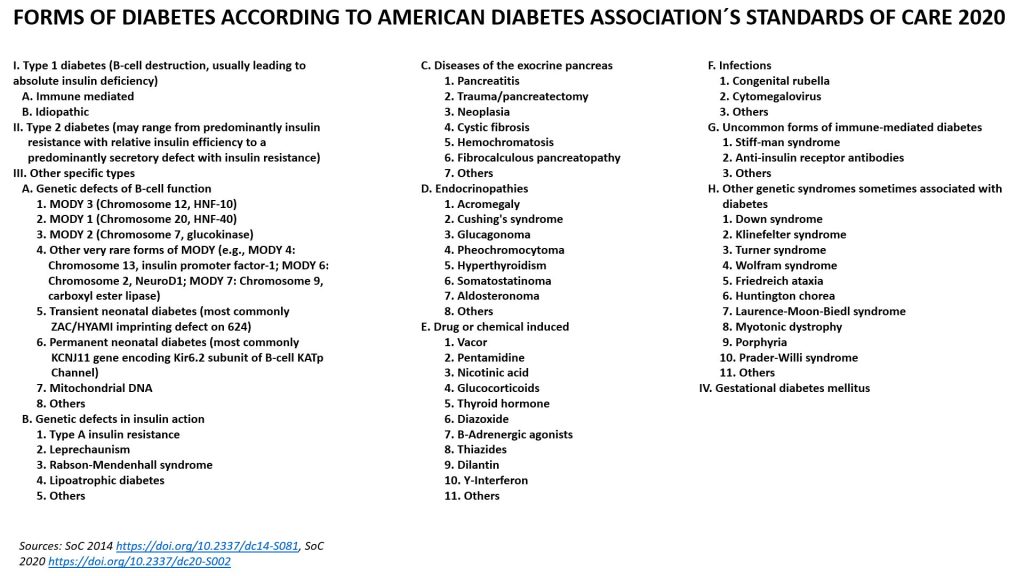
L’image en haut de cette page montre les formes les plus courantes de diabète avec d’autres mots, voici une version plus complète incluant tout ce que nous savons aujourd’hui, des Standards de Pratique 2020 et 2014 de l’American Diabetes Association (https://doi.org/10.2337/dc14-S081, SoC 2020 https://doi.org/10.2337/dc20-S002):
Prévalence du diabète en France
- Environ 3,5 millions de personnes (5,3% de la population) ont été traitées pour le diabète en 2020.
- La prévalence générale du diabète chez les adultes est estimée à 8,6%, ce qui correspond à près de 3,94 millions de cas.
- Des disparités géographiques existent, avec des taux plus élevés observés dans les régions du nord-est de la France.
DIABÈTE AUTOIMMUNE
Le diabète de type 1 et LADA (Diabète Autoimmune Latent chez les Adultes, début plus lent du diabète autoimmun chez les personnes de plus de ~35 ans) sont des maladies autoimmunes, ce qui signifie que le système immunitaire attaque par erreur les tissus sains du corps (1, 2). La seule chose attaquée sont les cellules beta dans les îlots de Langerhans dans le pancréas, et cela conduit à une carence absolue en insuline. Vous ne pouvez pas survivre sans insuline. Exemples d’autres maladies autoimmunes : arthrite rhumatoïde, sclérose en plaques et syndrome de Guillain-Barré. L’étiologie du diabète autoimmun est inconnue (novembre 2018), nous savons que les gènes de risque sont incontournables, mais on pense que ~30-50% du risque est dû à l’hérédité (3). Ce risque est principalement lié à la région HLA sur le chromosome 6, avec la plus grande association avec les haplotypes de classe HLA 2 DR3-DQ2 et DR4-DQ8. Ces gènes sont courants dans les pays nordiques, environ 20-25% de la population en possède un de ces gènes. Les biomarqueurs pour le diagnostic sont, en plus des gènes de risque, un faible C-peptide (excepté pour LADA, où le C-peptide au diagnostic peut être similaire à celui d’une personne ayant un diabète de type 2, mais diminue plus rapidement que pour le type 2) et des auto-anticorps. Les auto-anticorps peuvent être détectés des années avant le diagnostic et les symptômes d’une maladie. Peu d’informations sont disponibles sur la progression depuis l’apparition de l’auto-immunité jusqu’au diagnostic, sauf que plus il y a d’auto-anticorps en général, plus le risque de diabète auto-immun est élevé, et que le temps entre l’auto-immunité et le diagnostic est plus court (4). Il semble également que la progression soit plus agressive chez les enfants que chez les adultes. Le plus long temps connu pour une personne avec des auto-anticorps détectés jusqu’au diagnostic provient de Finlande. Une femme avait des auto-anticorps à l’âge de 11 ans et a été diagnostiquée à 32 ans (5). Il existe aujourd’hui cinq auto-anticorps connus (6, 7) même si la valeur de la dernière découverte, Tetraspanin 7, est inconnue.
Les chercheurs observent un lien assez fort avec les entérovirus, un groupe de ~100 virus, dont le virus coxsackie b (CBV) est un petit sous-groupe avec 6 virus différents. Si le CBV est impliqué, nous ne le savons pas, mais de nombreuses études ont observé une corrélation. Un essai chez l’homme débutera en Finlande en 2018 avec un vaccin contre le CBV. Si cela fonctionne, l’idée n’est pas un traitement, mais espérons-le, une possibilité de prévention (8). Au printemps 2018, un groupe de scientifiques de Cincinnati Children’s Hospital Medical Center, avec une méthode computationnelle (9), a démontré un lien avec sept maladies auto-immunes et le virus d’Epstein-Barr (EBV). L’EBV a été un candidat virus même si une corrélation plus forte a été observée avec d’autres virus. L’hypothèse aujourd’hui est que des facteurs environnementaux sont impliqués dans le processus comme “déclencheurs”, si tel est le cas, cela reste inconnu. Le diabète auto-immun est une maladie hétérogène, il pourrait y avoir différents “déclencheurs” selon l’âge au diagnostic, quels auto-anticorps apparaissent et peut-être d’autres facteurs. Le diabète auto-immun est chronique et ne peut aujourd’hui pas être prévenu, même si des biomarqueurs sont détectés. Cela peut survenir à tout âge. Le traitement est l’insuline avec MDI (Injections Quotidiennes Multiples, seringues) ou une pompe à insuline.
Le diabète de type 1 en France représente une proportion plus petite des cas par rapport au type 2. Des données récentes indiquent qu’il y a environ 14 700 nouveaux cas chaque année parmi les enfants et les adolescents âgés de 0 à 19 ans.
Références :
- https://www.nature.com/articles/nrdp201716
- https://doi.org/10.1007/s00125-015-3789-z
- http://care.diabetesjournals.org/content/38/10/1964
- https://www.ncbi.nlm.nih.gov/pubmed/28597949
- http://care.diabetesjournals.org/content/33/6/1206.long
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4407751/
- https://www.ncbi.nlm.nih.gov/pubmed/27221092
- https://www.uta.fi/en/news/story/preventive-vaccine-type-1-diabetes-be-studied-humans-first-time
- https://www.nature.com/articles/s41588-018-0102-3
DIABÈTE DE TYPE 2
L’étiologie derrière le diabète de type 2 est la génétique et les facteurs liés au mode de vie. L’hérédité est plus forte pour le diabète de type 2 que pour le diabète de type 1 (1, 2). Il est établi qu’environ 90 % sont obèses, mais cela signifie que tous ne le sont pas (3). Au Royaume-Uni, 12,4 % des personnes âgées de 18 ans et plus souffrant d’obésité ont un diabète diagnostiqué, cinq fois plus que les personnes ayant un poids santé, mais tous les personnes obèses ne développent pas le diabète de type 2, même si certains peuvent avoir une prédiabète (4). Beaucoup deviennent résistants à l’insuline et certains ont un syndrome métabolique (5). Un domaine de recherche passionnant ces dernières années est l’épigénétique, dont beaucoup reste encore inconnu (6, 7). Le “mode de vie occidental” n’est bien sûr pas le seul à blâmer pour l’augmentation de la prévalence du diabète de type 2, mais l’environnement dans lequel nous vivons n’aide certainement pas les gens à faire les meilleurs choix. Nous devons travailler ensemble pour changer la stigmatisation, cela n’aide pas les personnes obèses ou ayant un diabète de type 2 si la société leur dit “blâmez-vous”. À considérer également, le diabète de type 1 a une mortalité plus élevée et est une maladie plus grave, mais cela ne signifie pas que le diabète de type 2 est inoffensif. Ce n’est pas noir ou blanc.
Des chercheurs l’année dernière ont soutenu que le diabète de type 2 est une maladie hétérogène, encore plus que le diabète de type 1, et une sous-catégorisation a été proposée (8, 9). Cela est encore loin d’être accepté. L’idée est bien sûr la médecine de précision, pour donner le meilleur traitement et résultat possible. D’un autre côté, certains chercheurs estiment que les gens sont effectivement hétérogènes, mais pas le diabète de type 2 : il s’agit toujours de trop de graisse. Parmi plusieurs essais prometteurs, la recherche de Roy Taylor et al, réalisée au Royaume-Uni, est jusqu’à présent la plus intéressante. Ils ont publié un résultat remarquable dans The Lancet en décembre 2017 (10) où les participants (au total 306, intervention 149) avaient une durée maximale de 6 ans et n’étaient pas traités par insuline. L’intervention était : “L’intervention comprenait le retrait des médicaments antidiabétiques et antihypertenseurs, un remplacement total du régime (régime à 825–853 kcal/jour pendant 3–5 mois), une réintroduction progressive des aliments (2–8 semaines), et un soutien structuré pour le maintien à long terme de la perte de poids. Résultat principal : “Les résultats co-principaux étaient une perte de poids de 15 kg ou plus, et la rémission du diabète, définie comme une hémoglobine glyquée (HbA1c) inférieure à 6,5 % (<48 mmol/mol) après au moins 2 mois sans tous les médicaments antidiabétiques, de la ligne de base à 12 mois.” Résultat incroyable, la rémission du diabète a été atteinte chez 68 participants (46 %) qui avaient arrêté les médicaments antidiabétiques. Dans une analyse ultérieure et plus approfondie, ils ont examiné ce qui s’est passé, et ont découvert que la rémission nécessite une diminution de la graisse hépatique et pancréatique mais est dépendante de la capacité de récupération des cellules bêta (11). Lors du suivi après deux ans, 53/149 (35,6 %) de ceux ayant commencé l’intervention et 5/149 (3,4 %) dans le groupe témoin avaient eu une rémission, et 11,4 % (17/149) de l’intervention et 2 % (3/149) du groupe témoin avaient une perte de poids ≥15 kg. Parmi ceux maintenant une perte de poids ≥10 kg (45/272), 64 % (29/45) ont atteint la rémission (12). REMARQUE : C’est un régime très restrictif et ne doit en aucun cas être mis en œuvre sans consulter votre endo. C’est expérimental et bien que prometteur, pas encore largement accepté. Veuillez également vous rappeler que les participants à l’étude n’utilisaient pas encore d’insuline.
Bien que le mode de vie ne soit pas le seul responsable et que la génétique ait un impact, le diabète de type 2 est hautement préventable. Les études montrent des résultats différents, le programme de prévention du diabète a montré qu’une intervention intensive sur le mode de vie pourrait réduire l’incidence du diabète de type 2 de 58 % sur 3 ans (13). Néanmoins, plus d’actions sont nécessaires pour aider les gens à prendre des décisions plus rationnelles et meilleures. Le traitement actuel du diabète de type 2 consiste en des changements de mode de vie, des médicaments et après quelques années avec la maladie, la plupart des gens ont besoin d’insuline (14). Ainsi, malgré des résultats prometteurs dans les essais, le diabète de type 2 reste une maladie chronique sans guérison.
C’est la forme la plus répandue, représentant environ 93 % des cas de diabète en France. Elle est principalement liée à des facteurs de mode de vie tels que l’obésité et le comportement sédentaire. Les complications liées au diabète de type 2 sont plus fréquentes que celles du type 1, avec des hospitalisations nettement plus élevées pour les patients traités par insuline.
Références :
- https://www.niddk.nih.gov/health-information/diabetes/overview/what-is-diabetes/type-2-diabetes
- https://professional.diabetes.org/sites/professional.diabetes.org/files/media/type_2_1.pdf
- http://sciencenordic.com/slim-and-healthy-people-also-get-type-2-diabetes
- https://www.gov.uk/government/uploads/system/uploads/attachment_data/file/338934/Adult_obesity_and_type_2_diabetes_.pdf
- https://www.nhs.uk/conditions/metabolic-syndrome/
- http://www.ludc.med.lu.se/news-archive/epigenetic-changes-could-explain-type-2-diabetes/
- http://onlinelibrary.wiley.com/doi/10.1111/jdi.12724/pdf
- http://www.thelancet.com/journals/landia/article/PIIS2213-8587(18)30051-2/fulltext?elsca1=tlpr
- https://www.medscape.com/viewarticle/893305
- https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(17)33102-1/fulltext
- https://www.cell.com/cell-metabolism/fulltext/S1550-4131(18)30446-7#secsectitle0020
- https://www.directclinicaltrial.org.uk/Pubfiles/Final%20accepted%20draft,%20prior%20to%20editing%20and%20corrections.pdf
- http://care.diabetesjournals.org/content/41/Supplement_1/S51
- https://emedicine.medscape.com/article/117853-treatment
DIABÈTE MONOGÉNIQUE
Le diabète monogénique est plusieurs formes de diabète résultant d’une mutation dans un seul gène. La forme la plus courante de diabète monogénique est le MODY (diabète d’apparition à l’âge adulte chez les jeunes), qui représente 1 à 6 % du diabète pédiatrique. Jusqu’à présent, six formes différentes de MODY ont été identifiées, et celles-ci représentent 87 % des cas de MODY au Royaume-Uni (1). Certaines études suggèrent qu’il pourrait y avoir quatorze formes mais cela reste à confirmer. Cela signifie qu’il y a certains gènes à identifier. La caractéristique est que la plupart des personnes diagnostiquées ont moins de 25 ans, l’un des parents a la maladie (forte hérédité) et la plupart des gens n’ont pas besoin d’insuline. La plupart des gens conservent une production d’insuline, à différents degrés, mais ont une sécrétion limitée. Le traitement est généralement un régime ou des comprimés. Le MODY est parfois confondu avec le diabète de type 1 ou 2, ce qui pourrait être évité par un test génétique. Un diagnostic correct avec le bon traitement est bien sûr important pour le meilleur résultat possible.
D’autres formes monogéniques de diabète sont le diabète néonatal (une forme rare avec une incidence d’environ 1/100 000 naissances), une forme rare avec résistance à l’insuline due à un défaut génétique et d’autres (1, 2, 3).
Références :
- https://www.diabetesgenes.org/what-is-mody/
- https://www.niddk.nih.gov/health-information/diabetes/overview/what-is-diabetes/monogenic-neonatal-mellitus-mody
- https://ghr.nlm.nih.gov/condition/maternally-inherited-diabetes-and-deafness#genes
DIABÈTE GESTATIONNEL
Lors de la grossesse, environ 3-14 % des femmes deviennent résistantes à l’insuline (1). Certaines ne peuvent pas compenser avec une production accrue d’insuline et développent un diabète gestationnel. La plupart des gens parviennent à gérer grâce à des changements de mode de vie, mais certains ont besoin d’insuline. Les femmes qui ont eu un diabète gestationnel sont à risque de développer un diabète de type 2 (2), des études montrant cependant différents risques futurs.
Le diabète gestationnel affecte environ 8.8% des grossesses en France, posant des risques à la fois pour les mères et les nourrissons.
Références :
- https://emedicine.medscape.com/article/127547-overview#a2
- https://www.niddk.nih.gov/health-information/diabetes/overview/what-is-diabetes/gestational
DIABÈTE SECONDARY
De nombreux processus différents qui affectent le pancréas peuvent causer une réduction de la masse des cellules bêta et du diabète. La cause la plus courante de diabète secondaire, ou diabète de type 3c, est une pancréatite aiguë ou chronique récurrente, pancréas enflammé. Mais le cancer du pancréas, l’hémocromatose, la fibrose kystique, le traumatisme, l’infection sont également des raisons connues qui pourraient induire le diabète (1, 2, 3). La forme la plus évidente de diabète secondaire est celle qui suit une résection chirurgicale partielle ou complète du pancréas (4).
En 2017, des chercheurs britanniques ont publié une étude dans Diabetes Care (5) qui a suscité beaucoup d’attention dans le monde entier. Les gros titres de nombreux médias étaient : « une nouvelle forme de diabète, le diabète de type 3c, a été découvert ». La forme n’est pas nouvelle et le nom 3c ne l’est pas non plus, comme vous le voyez dans les liens ci-dessus. Cependant, les chercheurs ont découvert lors d’une analyse de 30 000 Britanniques nouvellement diagnostiqués avec le diabète que 559 personnes avaient un diabète de type 3c. Parmi eux, ~90% étaient mal diagnostiqués avec un diabète de type 2 et quelques-uns avec un diabète de type 1. Donc, le nombre absolu de personnes était faible. En effet, cela est très important pour la médecine de précision et le meilleur traitement, et résultat. Beaucoup de ces patients nécessitent en fait de l’insuline dès le départ. Les chercheurs ont constaté que le diabète de type 3c était plus fréquent que le diabète de type 1 dans ce groupe et inquiètent en ce sens qu’un diagnostic plus précis est indispensable. En ce qui concerne la Suède, nous avons depuis des années l’étude ANDIS (6) avec des informations très détaillées aujourd’hui sur ~15 000 patients nouvellement diagnostiqués diabétiques, et la prévalence du diabète de type 3c est de 1,2%. L’étude britannique est intéressante et doit être répliquée. Il y a probablement des différences entre les pays aussi.
Références :
- http://apps.who.int/iris/bitstream/handle/10665/66040/WHO_NCD_NCS_99.2.pdf?sequence=1&isAllowed=y
- https://doi.org/10.1016/S2468-1253(16)30106-6
- http://care.diabetesjournals.org/content/37/Supplement_1/S81?ijkey=56c2101d40bc86f2dde6ee307378f3cc04ca67a3&keytype2=tf_ipsecsha
- https://doi.org/10.2337/db16-1477
- https://doi.org/10.2337/dc17-0542
- http://andis.ludc.med.lu.se/all-new-diabetics-in-scania-andis/
DIABÈTE DE TYPE 1b
Dans un sous-ensemble plus petit de patients, aucune réponse immunitaire ou auto-anticorps n’est détectée, et la cause de la destruction des cellules bêta est inconnue. Ces patients sont sujets à la cétoacidose, n’ont aucune preuve d’auto-immunité et la plupart sont d’ascendance africaine ou asiatique (1, 2). L’hérédité est forte et le diabète de type 1b n’est pas associé aux HLA. Le besoin de remplacement de l’insuline vient et s’en va chez les patients.
Références :
- http://care.diabetesjournals.org/content/37/Supplement_1/S81?ijkey=56c2101d40bc86f2dde6ee307378f3cc04ca67a3&keytype2=tf_ipsecsha
- https://www.nature.com/articles/nrdp201717
Stratégies de santé publique en France
Des efforts sont en cours pour s’attaquer à l’épidémie de diabète en France à travers :
- des campagnes de sensibilisation du public améliorées ;
- un meilleur accès aux services de santé préventifs ;
- une éducation tant pour les patients que pour les fournisseurs de soins de santé afin de réduire les complications et d’améliorer les stratégies de gestion.
En résumé, le diabète en France représente une préoccupation croissante en matière de santé, caractérisée par des taux de prévalence significatifs et divers types. Les initiatives de santé publique en cours visent à atténuer son impact grâce à de meilleures stratégies de gestion et de prévention.


























